Implication du cerveau et de la leptine dans le surpoids et l’obésité
Vincent Prevot est Directeur de recherches à l’Inserm sur le site du CHU de Lille. Il anime une équipe appelée Développement et plasticité du cerveau neuroendocrine. Son travail consiste à étudier le rôle de l’hypothalamus (une région du cerveau) dans le contrôle de 2 grandes fonctions : la reproduction et la prise alimentaire. Il analyse également comment ces 2 fonctions dialoguent entre elles.
Il a accepté de répondre à nos questions concernant l’implication d’une hormone dans le surpoids.
Cet article sera également publié chez SOPK Europe, où je suis chargée du comité scientifique. Bonne lecture !
Le surpoids : une maladie périphérique ou une maladie du cerveau ?
On s’aperçoit que la plupart des syndromes ou des maladies que l’on pensait être des maladies « périphériques » (des maladies d’un organe ou d’un tissu du corps), ont en réalité une origine au niveau du cerveau, on parle d’origine « centrale ». C’est le cas de l’obésité et du Syndrome des Ovaires Polykystiques (SOPK) par exemple.
Pour en savoir plus sur l’origine centrale du SOPK, je vous renvoie vers cet article.
L’obésité n’est donc pas seulement une maladie du tissu graisseux ou le SOPK une maladie des ovaires. Ces pathologies ont toutes les deux une origine centrale.
L’hypothalamus une région déterminante dans le cerveau pour le contrôle du poids
L’hypothalamus est situé à la base de notre cerveau.
C’est l’interface entre notre corps et le reste du cerveau. C’est la porte d’entrée de tous les signaux corporels qui doivent informer le cerveau sur l’état de notre organisme, afin de permettre à celui-ci de prendre de bonnes décisions pour réguler chacun de nos organes.
Le cerveau ainsi informé peut alors agir : soit en relarguant d’autres neurohormones, soit en agissant par le tronc cérébral et la moelle épinière.
Dans le cas de la régulation du poids, le cerveau reçoit un message en provenance du corps, et plus particulièrement du tissu graisseux : la leptine.
La leptine, hormone actrice dans la régulation du poids
Le tissu graisseux sécrète une hormone extrêmement puissante qui s’appelle la leptine.
Je rappelle que les hormones sont des « messagers chimiques » qui délivrent un message, une information et qui indiquent à notre corps comment fonctionner.
La leptine est une hormone « coupe faim » qui contrôle l’appétit et la dépense énergétique. Elle est produite par le tissu adipeux (=tissu graisseux), circule dans le sang et transmet au cerveau, via l’hypothalamus, le signal de satiété. La sécrétion de leptine est proportionnelle aux réserves de graisses de l’organisme : ainsi, + j’ai de tissus gras, + je sécrète de la leptine.
La leptine a été découverte dans les années 90.
Un système d’autorégulation est normalement en place : plus on prend du poids, plus on a de masse graisseuse et plus on produit de leptine (« l’hormone coupe faim »). Ainsi, en théorie, sous l’action de la leptine, les personnes qui prennent du poids devraient davantage réguler leur appétit et diminuer leurs apports alimentaires pour retrouver petit à petit un poids de forme…
Mais c’est là que l’histoire se complique …
Pour être efficace, la leptine doit arriver correctement jusqu’au cerveau
C’est le paradoxe de l’obésité : la leptine est produite en grande quantité mais ne semble pas agir correctement au niveau du cerveau. C’est ce qu’on appelle une résistance centrale à la leptine périphérique.
Les études ont montré qu’une alimentation riche en graisses va altérer le transport de la leptine vers le cerveau.
Les chercheurs ont mené plusieurs expériences pour mettre en avant ce phénomène :
Expériences menées chez la souris : altération du transport de la leptine jusqu’au cerveau liée au surpoids
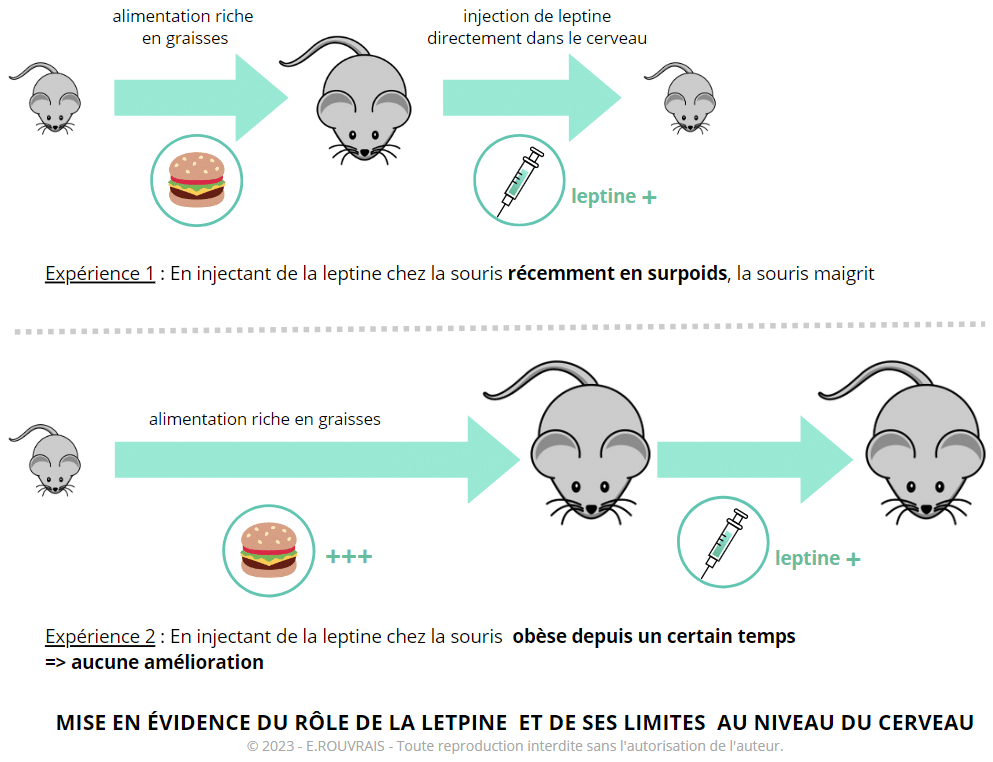
Expérience 1 : Pendant 8 semaines, une alimentation riche en graisses est donnée aux souris. Les souris grossissent et ne perçoivent plus le signal de la leptine.
Si on injecte directement la leptine au niveau de leur cerveau, alors les souris retrouvent le signal de satiété et mincissent à nouveau.
Expérience 2 : Si l’on poursuit l’alimentation riche en graisses chez ces souris pendant 15 semaines, le système devient complètement dysfonctionnel. Que l’on injecte de la leptine en périphérie ou dans le cerveau cela ne fonctionne plus (la souris ne maigrit pas). On parle alors de résistance totale à la leptine.
Expériences menées chez l’homme : en cas de surpoids ou d’obésité, la leptine n’accède pas correctement au cerveau
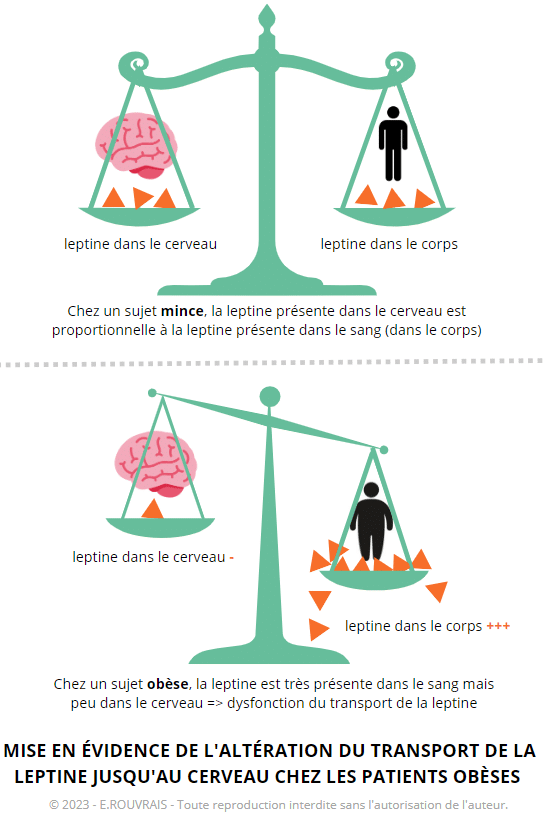
Les chercheurs ont mené d’autres expériences en mesurant le rapport entre la leptine circulant dans le corps (dans le sang) et la leptine présente dans le liquide céphalo rachidien (au niveau du système nerveux).
- Chez le patient mince : le rapport est linéaire : + il y a de leptine dans le sang, + il y en a dans le cerveau.
- Chez le patient obèse : il n’y a pas de corrélation : il y a beaucoup de leptine dans le sang et finalement assez peu au niveau du cerveau => ce qui montre que c’est bien un problème de passage de la leptine dans le cerveau.
Expériences menées chez le porc, montrant l’impact néfaste d’une mauvaise alimentation sur le transport de la leptine jusqu’au cerveau
Des études ont également été réalisées chez le porc : avec un panel de porcs nourris avec une alimentation équilibrée pendant 10 semaines et un autre panel nourri avec une alimentation riche en graisses pendant 10 semaines.
Résultat : en seulement 10 semaines d’une alimentation riche en graisses, le poids du porc a doublé, et sa sécrétion de leptine dans le sang a fortement augmenté.
Au fil des semaines, les chercheurs ont mesuré le passage de la leptine dans le système nerveux du porc. Ils ont mis en évidence que très rapidement (dès 4 semaines seulement d’alimentation riche en graisses), le passage de la leptine dans le cerveau devient dysfonctionnel.
En conclusion, dès que le surpoids devient significatif, le passage de la leptine dans le cerveau commence à être altéré.

L’équipe de chercheurs, dirigée par Vincent Prevot, s’est alors penchée sur la question suivante : Quel est le point d’entrée de la leptine dans notre cerveau ?
Les tanycytes, porte d’entrée de la leptine dans le cerveau
Le cerveau est précieux, il doit être bien protégé de potentielles molécules toxiques. C’est la barrière hématoencéphalique qui assure ce rôle de « barrière infranchissable ».
On peut imaginer que le cerveau est comme protégé par un « coffre-fort ».

Mais en réalité, il existe toutefois 5 endroits très confidentiels dans le cerveau, à travers lesquels il peut recevoir des informations en provenance de la périphérie (du corps).
Parmi eux, on trouve « l’éminence médiane », une zone située dans l’hypothalamus. L’hypothalamus joue un rôle important dans la régulation de différents mécanismes physiologiques. À son niveau, la fonction barrière est assurée par des cellules bien singulières qu’on appelle des tanycytes.
Les tanycytes permettent l’échange d’informations entre le cerveau et le reste du corps (la périphérie). Les échanges se font dans les 2 sens.
A la manière d’un « ascenseur » qui monte et qui descend, les tanycytes permettent :
- La montée d’informations, en provenance du corps vers le cerveau : par exemple, l’hormone leptine qui permet d’informer le cerveau que l’on n’a plus faim, lorsque l’ascenseur est fonctionnel.
- La descente d’information du cerveau vers le corps : prenons un tout autre exemple avec l’hormone GnRH, sécrétée par l’hypothalamus et qui permet d’orchestrer le cycle féminin.
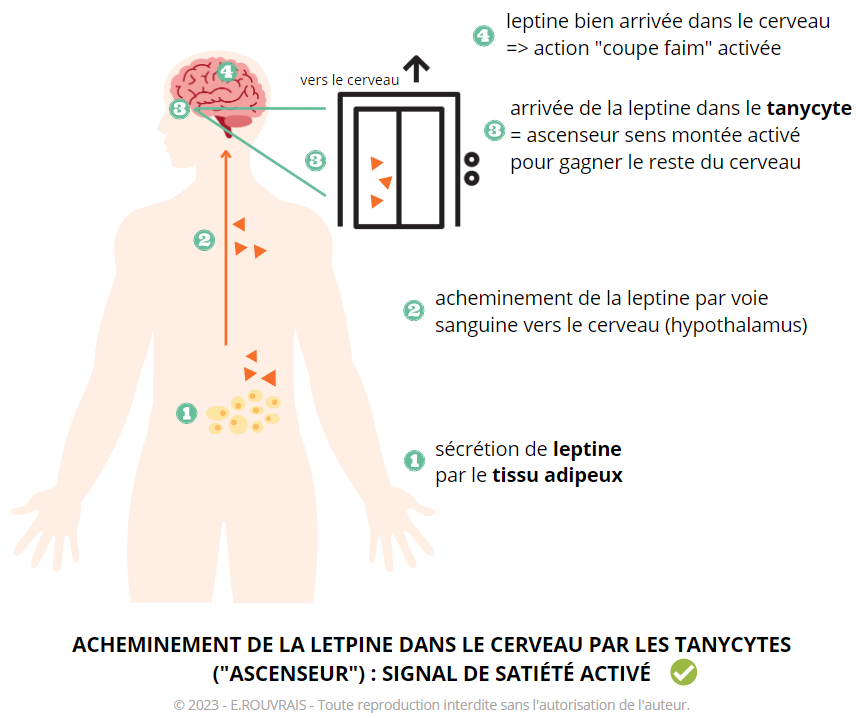
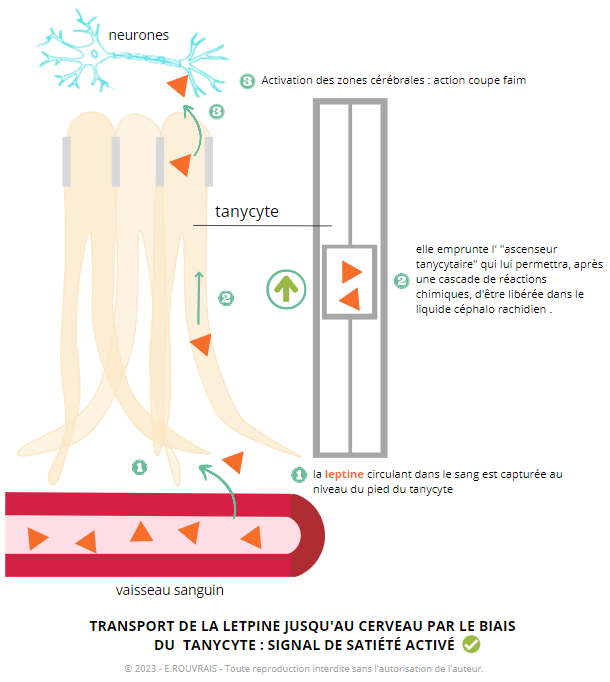
Lorsque le système est fonctionnel, la leptine est sécrétée par le tissu adipeux (=graisseux) et gagne la région de l’hypothalamus par le biais du système sanguin. Une fois arrivé à ce niveau, la leptine emprunte l’ « ascenseur tanycytaire » dans le sens de la montée : le départ commence sur le bord extérieur du cerveau et l’ascension se finit au niveau du liquide céphalo rachidien. La leptine gagne bien le cerveau et peu ainsi transmettre efficacement son message de sensation de satiété, permettant une bonne régulation du poids.
Acheminement de la leptine jusqu’au cerveau par l’ascenseur des tanycytes
Lorsque le système est fonctionnel
La leptine se lie à un récepteur dans les pieds du tanycyte. Elle sera ensuite capturée dans ce dernier et activera une cascade de réactions chimiques permettant de la relarguer au niveau du cerveau.
Lorsque le système devient dysfonctionnel en cas de surpoids ou d’obésité
En cas d’obésité, la leptine rentre dans le pied du tanycyte mais ne fait pas son ascension jusqu’au cerveau. Si nous reprenons l’analogie de l’ascenseur, cela reviendrait à dire que la leptine reste bloquée au Rdc. Par conséquent, le message ne parvient pas au cerveau : ce qui induit une mauvaise signalisation du sentiment de satiété et donc des difficultés dans le contrôle du poids.
Dans le cas d’une obésité importante et prolongée, la leptine reste « coincée dans l’ascenseur » (dans le pied du tanycyte) mais paradoxalement des « fuites » peuvent également exister, exposant ainsi certaines neurones à un excès de leptine. Les neurones ayant été exposés à ce surplus de leptine, du fait de l’obésité, deviennent insensibles à cette hormone. On parle alors de résistance totale à la leptine. On pourrait simplifier en une phrase : « trop d’informations tue l’information ».
Vers des perspectives thérapeutiques
Les chercheurs ont découvert très récemment que la cascade de réactions chimiques permettant l’ascension de la leptine dans le tanycyte pouvait être réactivée chez les souris obèses grâce à un traitement spécifique. Cela permet à la leptine d’atteindre de nouveau le cerveau et de retrouver progressivement un régime équilibré (1).
Plusieurs essais cliniques sont également en cours chez l’homme et la femme, notamment le test d’une molécule qui permettrait la restauration du transport de la leptine chez les patients en situation d’obésité.
Cela offre des perspectives de nouveaux traitements chez les personnes en surpoids qui permettraient de restaurer le passage de la leptine dans le cerveau, avant que ce dernier ne devienne complètement résistant à cette hormone.
Lien avec le Syndrome des Ovaires Polykystiques (SOPK)
Le surpoids et les problématiques métaboliques sont omniprésents dans le SOPK. Beaucoup de femmes avec un SOPK souffrent de surpoids, d’obésité, de résistance à l’insuline et parfois même de diabète.
La leptine en plus d’avoir une action sur le contrôle du poids agirait également sur la capacité du pancréas à percevoir le glucose (2) et donc à sécréter l’insuline en retour. Ce qui est une découverte importante pour toutes les personnes diabétiques ou insulinorésistantes.
D’autre part, il a été montré que l’un des types cellulaires qui exprime le plus le récepteur à l’AMH (Hormone Anti Müllerienne) est le tanycyte. On sait que dans le SOPK, l’AMH est souvent élevée et pourrait être en lien avec : le développement de la pathologie et de ses symptômes (hyperandrogénie) ainsi que dans la transmission du SOPK de la mère à l’enfant.
En d’autres termes : les tanycytes sont donc sensibles à l’AMH et cela pourrait probablement expliquer les problématiques métaboliques et de surpoids mais aussi les pulsations accrues de GnRH qui sont communes chez les femmes atteintes du SOPK (et en lien avec les symptômes d’hyperandrogénie et de troubles du cycles menstruel).
Il se pourrait que l’AMH entraine la rétraction des pieds tanycytaires favorisant ainsi une hypersécrétion de GnRH.
Par rapport au cycle menstruel en général, il a été également montré que les œstrogènes potentialisent le transport de la leptine. Cela pourrait également expliquer qu’en première partie du cycle, lorsqu’il y a beaucoup d’œstrogènes, certaines femmes mangent moins.
D’autres liens encore
Le transport tanycytaire fonctionnel (l’ascenseur qui fonctionne correctement) est en lien avec une bonne gestion de l’appétit et une bonne régulation du poids, mais aussi avec le bon fonctionnement du pancréas, la fonction de reproduction et un bon vieillissement. Les études montrent également que les tanycytes pourraient être en lien avec des problématiques thyroïdiennes et l’anorexie.
Source :
(1) https://presse.inserm.fr/le-mecanisme-de-la-satiete-decrit-et-restaure-chez-la-souris/10995/


No Comments