Dans le cadre de mon engagement pour l’Association SOPK Europe, je me suis récemment rendue à Lille pour retrouver Emelyne, vice présidente de l’association.
Ensemble, nous avons interrogé le Docteur Paolo Giacobini, Directeur de recherche à l’Inserm, pour nous éclairer sur les avancées de la science concernant le Syndrome des Ovaires Polykystiques (SOPK). Voici la restitution de cet entretien ci-dessous.
Le Dr Paolo Giacobini est spécialisé en neuro-endocrinologie et Biologie de la reproduction. Il travaille depuis plusieurs années sur le Syndrome des Ovaires Polykystiques (SOPK), et en particulier, sur la communication entre le cerveau et les ovaires dans l’acquisition des traits phénotypiques du SOPK.
Il mène également des recherches dans la transmission de la pathologie de mère en fille et tente de développer de nouveaux outils de diagnostic et thérapeutiques.
1. Origine et causes du SOPK
Le SOPK est dû à un dérèglement hormonal d’origine ovarienne (au niveau des ovaires) et central (au niveau du cerveau).
Les Causes de ce dérèglement sont certainement multifactorielles :
- Génétique : transmission de caractères héréditaires (des parents à la descendance), portés par nos gènes et plus généralement par l’ADN.
- Épigénétique : modification de l’activité des gènes (activation ou inhibition) sans modification de la séquence d’ADN.
- Environnemental : exposition aux perturbateurs endocriniens par exemple.
Avant d’aller plus loin, revenons sur quelques notions de génétique en biologie.
2. Génétique
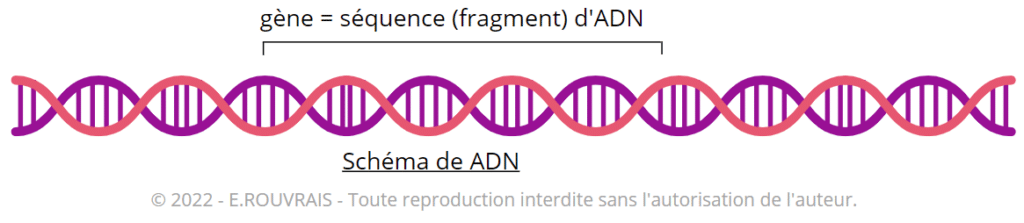
a) ADN et séquences d’ADN (gènes)
Notre corps est constitué entièrement de cellules : ce sont les unités de base de tout organisme animé.
Les différentes cellules de notre organisme contiennent, au sein de leur noyau, un même exemplaire de notre ADN (c’est – à – dire nos données génétiques, héritées de nos parents). L’ADN est une très grande chaîne moléculaire formée de différentes séquences que l’on appelle des gènes.
Chaque gène est une sorte de « code » qui permettra ensuite la synthèse d’une protéine au sein de la cellule.
Ces protéines sont les composantes, « les briques de construction », qui seront à l’origine de tous les tissus et organes du corps humain.
b) Comment nos gènes s’expriment-t-ils ?
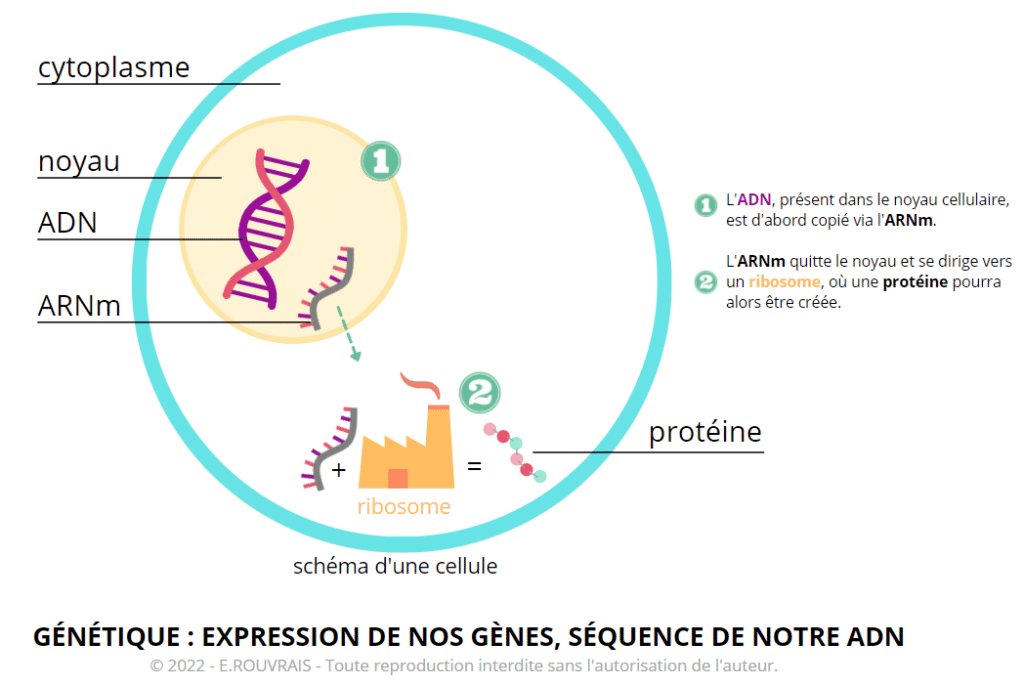
L’ADN, encapsulé dans le noyau de nos cellules, renferme toutes les informations nécessaires au développement, à la survie et à la reproduction de notre organisme. C’est un petit peu notre « code source ». Comme évoqué juste avant, notre ADN reste dans le noyau de nos cellules.
Pour que nos gènes puissent s’exprimer et aboutir à la synthèse de protéines, il va falloir faire une copie de notre ADN. L’ADN est d’abord copié dans le noyau de nos cellules sur un brin d’ARN messager (ARNm). L’ARNm quitte ensuite le noyau pour entrer dans le cytoplasme de la cellule. Il pourra alors se coupler à une usine de production de protéines, appelée ribosome. L’ARNm sera traduit dans l’usine et permettra la création d’une protéine.
Les protéines jouent un rôle essentiel. Elles forment notre phénotype, c’est-à-dire l’ensemble de nos caractéristiques visibles, codés par un ou plusieurs gènes. Par exemple, certains gènes déterminent la couleur de la peau, des cheveux, des yeux, etc. Notre corps fabriquera, suivant la présence ou non de certains gènes, différentes protéines qui pourront donner des phénotypes variés : couleur de yeux suivant (avoir les yeux bleus par exemple).
Nous venons de décrire comment notre ADN, nos gènes, notre « génétique » s’expriment et donnent à voir certains de nos traits physiques observables… mais l’histoire ne s’arrête pas là… Nous ne sommes pas que le produit de nos gènes, nous ne sommes pas déterminés uniquement par un « programme ou code génétique », hérité de nos ancêtres. Il existe également d’autres mécanismes appelés épigénétiques.
3. L’épigénétique, qu’est-ce que c’est ?
L’épigénétique met en lumière ou non des gènes portés par notre ADN. A la manière d’un interrupteur ON/OFF, les mécanismes épigéniques vont activer ou désactiver l’expression de certains de nos gènes, sans modifier notre ADN. Les marques épigénétiques vont permettre de moduler l’expression des gènes sans changer leur séquence. Il s’agit d’une machinerie complexe, faisant appel par exemple à la fixation d’« étiquettes biochimiques » un peu partout sur notre ADN, qui va rendre les gènes accessibles au processus de lecture, ou au contraire en bloquer le mécanisme.
Nous nous concentrerons ici uniquement sur le processus de méthylation, qui empêche en quelque sorte la lecture d’une partie de notre ADN (et donc la création de la « copie » 1ère étape nécessaire à la synthèse des protéines), et donc l’expression de certains gènes et la synthèse de protéines.
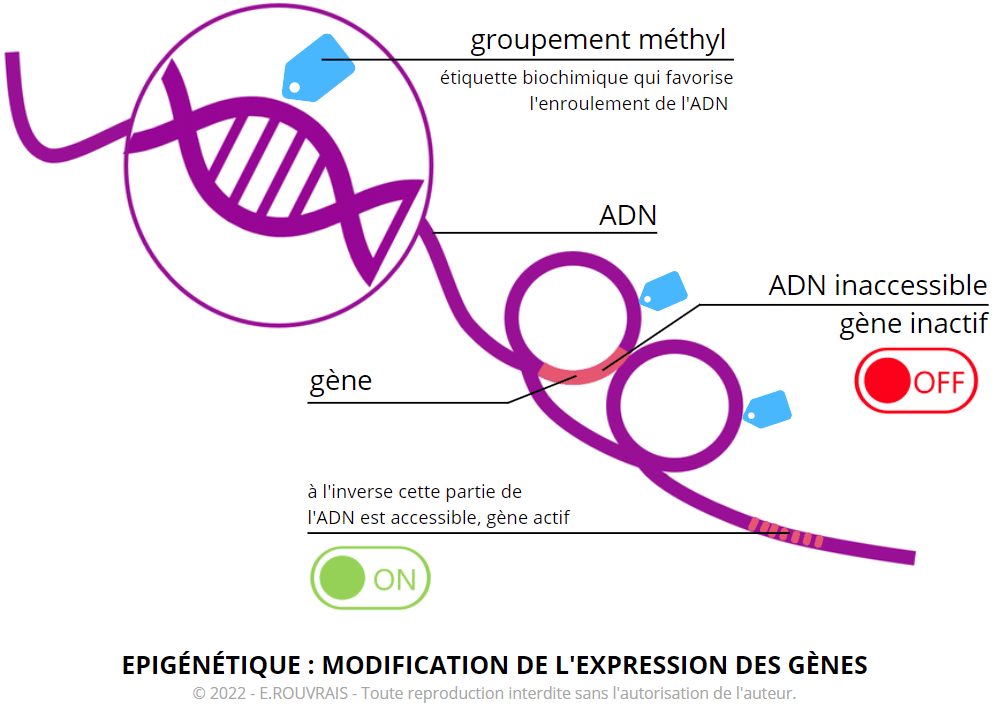
Dans le processus de méthylation, l’étiquette biochimique est appelée groupement « méthyle » (CH3), c’est une molécule constituée d’un atome de carbone et de 3 atomes d’hydrogène.
Pour faire simple, le groupement méthyle peut se fixer comme une étiquette sur notre ADN et favoriser l’enroulement de cette dernière. Si un fragment d’ADN est enroulé, alors cette partie ne peut plus être lue, le gène ne pourra plus s’exprimer : il est rendu silencieux (interrupteur en position OFF).
Les modifications épigénétiques sont induites par notre environnement au sens large. Nos comportements quotidiens – notre alimentation, l’exercice que l’on pratique, notre résistance au stress, le tabagisme, une maladie, le style de vie que l’on adopte – peuvent conduire à des modifications dans l’expression de nos gènes, sans affecter leur séquence.
Le phénomène peut être transitoire, mais il existe des modifications épigénétiques pérennes, qui persistent lorsque le signal qui les a induites disparaît. Les marques épigénétiques peuvent être transmises au cours des divisions cellulaires et d’une génération à l’autre, selon des mécanismes encore mal compris à l’heure actuelle.
4. Epigénétique et nouveaux traitements pour le SOPK ?
Le Dr Paolo Giacobini et son équipe ont travaillé sur des souris pour mettre en évidence l’implication des mécanismes épigénétiques dans la physiopathologie du caractère épigénétique du SOPK.
a) L’expérience chez les souris
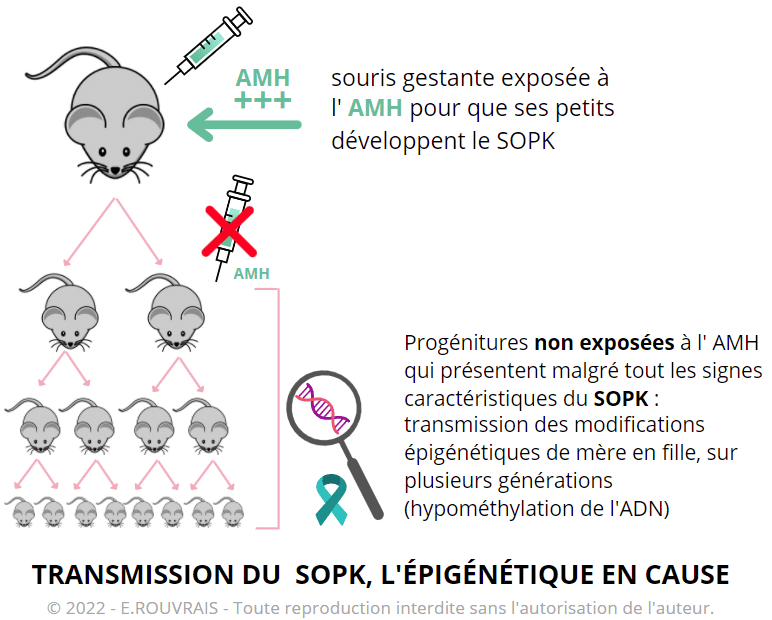
Des souris en gestation ont été exposées à un excès d’Hormone Anti-Mullérienne (AMH), afin d’entrainer l’apparition d’un SOPK chez leur progéniture. En effet, un excès d’AMH est en lien avec le SOPK (nous détaillons ce point-là au paragraphe n°5)
Les animaux ont ensuite été croisés sur trois générations, sans nouvelle exposition à de l’AMH.
b) Résultat de l’expérience
À chaque génération, toutes les femelles qui sont nées présentaient les symptômes caractéristiques du SOPK : un taux élevé de testostérone circulant, une infertilité en rapport avec des troubles de l’ovulation et des désordres métaboliques.
Les scientifiques ont identifié plusieurs gènes chez les souris SOPK dont l’expression diffèrerait de ceux observés chez des animaux sains. Les chercheurs ont également mis en évidence chez les souris SOPK un déficit en marques épigénétiques : une baisse de la méthylation (on parle d’hypométhylation). Rappelons-nous la méthylation permet d’inhiber l’expression de certains gènes, sans altérer l’ADN.
c) Conclusion
Pour Paolo Giacobini et son équipe, l’excès d’AMH chez les souris de la génération 0 (lors de la gestation) est responsable de l’apparition de modifications épigénétiques transmissibles, qui conduiraient à l’apparition des symptômes de SOPK sur plusieurs générations. Ces modifications épigénétiques ont également été retrouvées chez les femmes atteintes du SOPK.
d) Vers un nouveau traitement pour la femme : thérapie épigénique ?
Pour restaurer les processus épigénétiques, une thérapie épigénétique basée sur l’utilisation d’un donneur de groupe méthyle, issu d’un extrait naturel végétal (rappelons-nous la petite étiquette bleue dans le schéma sur l’épigénique) – est administré chez la souris SOPK, sous forme de complément alimentaire.
Résultat clinique : Chez la souris, l’efficacité de ce traitement a été démontrée : le complément alimentaire (qui ajoute des groupes méthyles sur l’ADN) est capable de changer l’expression de certains gènes, impliqués dans la fonction ovarienne (la reproduction), l’inflammation et le contrôle du métabolisme.
Pour la souris, le traitement est efficace mais qu’en est-il pour l’être humain ?
Les travaux des chercheurs offrent de nouvelles perspectives de diagnostics et thérapeutiques.
D’une part, ces marqueurs épigénétiques pourraient servir de signature pour dépister précocement le SOPK chez les petites filles à risque familial, avant leur puberté.
D’autre part, un traitement, à base d’extrait de plante médicalisé qui permet d’ajouter des groupes méthyles à l’ADN et ainsi restaurer le profil épigénétique, pourrait être envisagé chez certaines patientes. Il faut toutefois que les chercheurs poursuivent leurs études précliniques pour vérifier qu’il n’y a pas d’effets secondaires à long terme (ne pas toucher l’expression de certains gènes potentiellement dangereux chez la femme, et sans rapport avec leur fertilité).
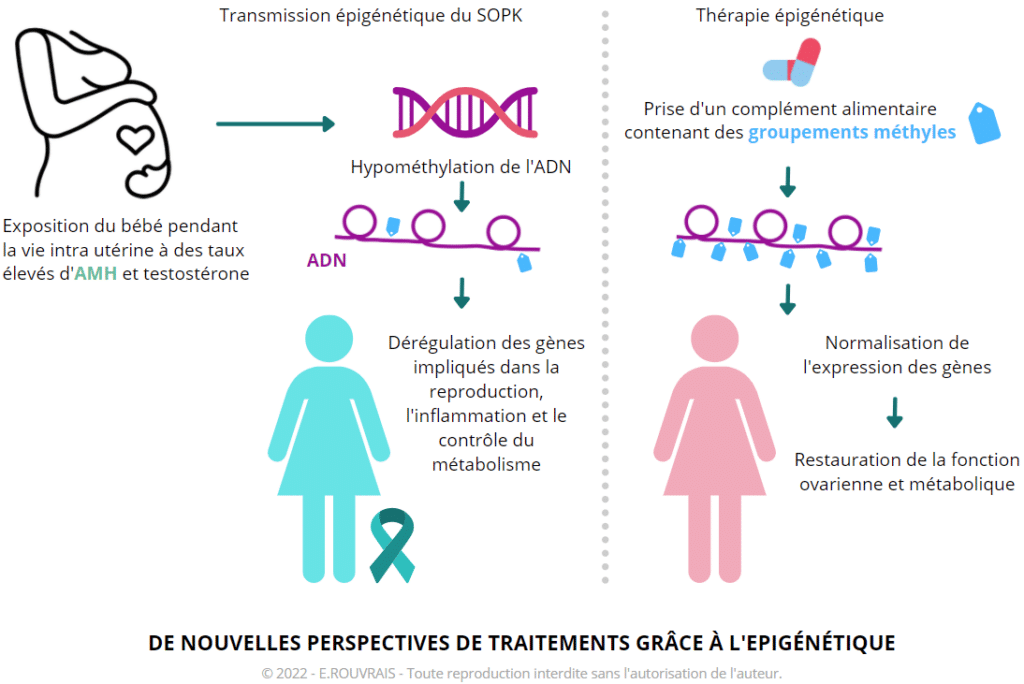
Le détail de ces recherches est accessible dans l’étude : Polycystic ovary syndrome is transmitted via a transgenerational epigenetic process(1). Le schéma ci-dessous est inspiré d’un graphique disponible dans cette étude.
Nous avons évoqué le caractère épigénétique du SOPK, qui peut être transmis de génération en génération, mais qui pourrait également être normalisé à l’aide d’une thérapie épigénétique. Il existe également d’autres pistes thérapeutiques pour soigner le SOPK. Le Dr Paolo Giacobini nous a informé des études en cours sur l’Hormone Anti-Mullérienne (AMH), responsable – si présente en excès – du SOPK.
5. Origine centrale du SOPK, AMH et nouvelles pistes thérapeutiques
L’AMH est une hormone sécrétée par les ovaires. Le corps scientifique a longtemps pensé que l’AMH n’avait qu’un impact sur les gonades (ovaires). Chez les femmes atteintes du SOPK, on retrouve souvent des taux élevés d’AMH (concentration 2 à 3 x supérieure).
Grâce aux travaux de recherche du Dr Paolo Giacobini, on sait aujourd’hui que l’AMH intervient également au niveau du cerveau.
a) Les études chez la souris
Les études précliniques (2) chez la souris montrent que l’AMH joue un rôle sur l’activation des neurones cérébraux à gonadotrophines (GnRH), responsables du contrôle de la reproduction.
Un taux élevé d’AMH provoquerait une véritable réaction en chaîne : un taux élevé d’AMH entraînerait une hyperexcitabilité des neurones à GnRH dans le cerveau, entraînant ainsi une sécrétion accrue de GnRH (par l’hypothalamus), augmentant à son tour la production d’Hormones Lutéinisantes ou LH (par l’hypophyse) et seraient à l’origine de l’hyperandrogénie ovarienne retrouvée dans le SOPK
De plus, cette AMH élevée et/ou l’excès de testostérone pendant la période gestationnelle pourrait contribuer à la transmission du SOPK de la mère à l’enfant.
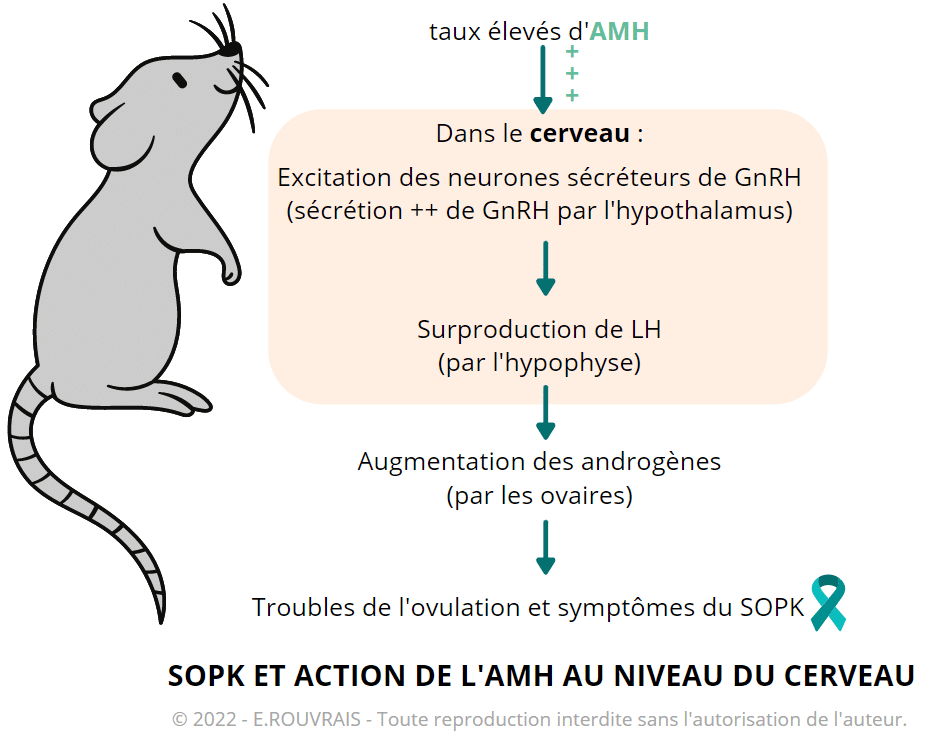
b) Vers un nouveau traitement pour la femme ?
La découverte du rôle central de l’AMH, et surtout de son action sur le cerveau, offre des perspectives de traitement pour le SOPK. Les chercheurs travaillent sur une thérapeutique de nouvelle génération qui permettrait de normaliser l’activité des neurones à GnRH ou de normaliser le taux d’AMH. Plusieurs pistes sont à l’étude :
- Le développement d’une molécule capable d’empêcher la liaison entre l’AMH et ses récepteurs sur les neurones à GnRH (objectif : normaliser l’activité des neurones à GnRH),
- L’utilisation d’antagonistes à la GnRH qui entrent en compétition avec les récepteurs hypophysaires à la GnRH et permettent de régulariser la sécrétion de LH,
- Un travail directement sur la normalisation de l’AMH.
Les études se poursuivent et sont très encourageantes car elles offrent une voie thérapeutique plus ciblée que les traitements actuels. Les médicaments proposés aujourd’hui, comme la pilule par exemple, sont anti-symptomatiques : ils traitent les conséquences du SOPK mais non la cause. Ils permettent notamment de traiter des symptômes comme l’hyperandrogénie mais ne parviennent pas aujourd’hui à agir sur l’origine de ce dérèglement hormonal. Aujourd’hui, chaque symptôme handicapant du SOPK doit être pris en charge un par un (il n’existe aucun traitement curatif global). Par exemple, on essaie de régulariser les hormones avec une pilule, de traiter l’acné avec des soins locaux, l’alopécie avec un autre traitement etc…
La promesse des traitements futurs ? Agir à la source du problème et permettre en réglant la cause originelle, une cascade vertueuse qui régulariserait l’ensemble du tableau clinique du SOPK.
6. Le SOPK ou des SOPKs pluriel ?
Nous avons échangé librement avec le Dr Paolo Giacobini sur nos interrogations concernant le SOPK. En effet, de manière très « simpliste », nous constatons qu’il n’existe pas « un profil type » de la femme atteinte du SOPK. Certaines sont minces, d’autres ont des rondeurs et éprouvent des difficultés à perdre du poids, d’autres encore présentent une résistance à l’insuline, avec ou sans troubles métaboliques associés. Les symptômes et les problématiques ne sont pas les mêmes d’une femme à l’autre et pourtant cela porte le même nom…
Si nous prenons l’exemple de la résistance à l’insuline :
Certaines femmes atteintes du SOPK présentent une résistance à l’insuline, d’autres non. Cette résistance à l’insuline peut augmenter la sécrétion de testostérone par les ovaires et donc être à l’origine des symptômes du SOPK (hyperandrogénie).
Mais qu’en est-il des femmes qui ont des symptômes d’hyperandrogénie sans aucune résistance à l’insuline ? S’agirait-il d’une autre « forme » de SOPK (avec une cause différente) ? Seraient-ce différentes pathologies réunies sous le même nom du SOPK ?
Il y a presque 20 ans, les médecins ont défini le SOPK sur les 3 critères suivants, basés essentiellement sur l’axe de la reproduction/fertilité : hyperandrogénie, trouble de l’ovulation et ovaires riches en follicules. A l’époque, ces critères ont permis d’établir les 4 phénotypes que l’on connait aujourd’hui : A, B, C et D.
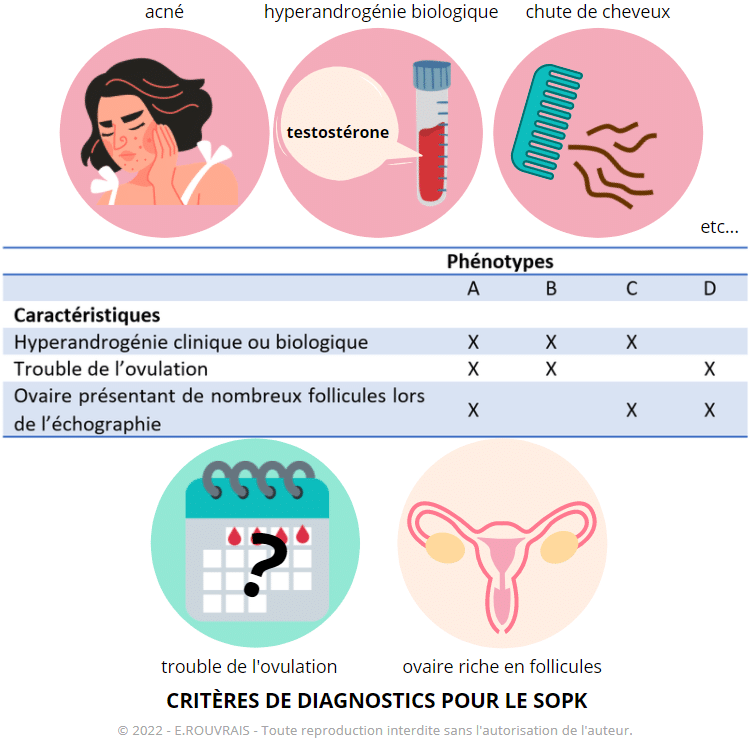
Le Dr Giacobini tente dans ses recherches d’aller encore plus loin et d’établir des critères supplémentaires qui permettraient de différencier les différentes formes de SOPK pour un meilleur diagnostic, une prise en charge médicale personnalisée, un travail de prévention amélioré et pourquoi pas de futurs traitements médicaux différents et ciblés,suivant le profil SOPK.
Il pourrait être intéressant par exemple d’y inclure : l’inflammation, les troubles métaboliques, la résistance à l’insuline, le taux d’AMH, l’exposition prénatale aux androgènes et le terrain psychologique (dépression, anxiété).
Pour simplifier, 2 profils « type » semblent se définir (mais encore une fois, il est difficile de tout généraliser), avec des causes et des problématiques différentes :
- Un profil SOPK de type « femme mince », avec une LH élevée et de nombreux follicules dans les ovaires dont l’origine serait au niveau du cerveau avec l’hyper excitation des neurones à GnRH (cf. paragraphe n°5)
- Un profil SOPK de type « femme en surpoids » avec une pathologie exacerbée par le biais de la prise de poids, en lien avec une résistance à l’insuline.
Suivant le profil SOPK et les différents critères de diagnostics (version modernisée), il pourrait y avoir une prise en charge ciblée et différents traitements médicaux proposés aux patientes.
Elargir les critères de diagnostic permettrait d’améliorer la coordination et la communication entre les différents professionnels du SOPK : gynécologue-endocrinologue-diabétologue et également d’obtenir une prise en charge globale.
7. Conclusion
La recherche française et internationale avance sur tous les plans :
- De nouveaux outils de diagnostic : Dans les années à venir, des marqueurs moléculaires, pourront probablement être recherchés, dans le sang par exemple, pour diagnostiquer de manière fiable et rapide le SOPK mais aussi pour anticiper les éventuelles complications dès le plus jeune âge (diagnostic précoce – avant la puberté- chez les petites filles à risque familial de développer un SOPK).
- De nouveaux outils thérapeutiques : le défi moderne consiste à trouver des traitements ciblés et personnalisés suivant le profil SOPK de chaque femme, qui n’agiront pas uniquement sur les symptômes du SOPK mais bien sur les causes réelles de ce dérèglement hormonal.
La recherche a considérablement avancé et les études se poursuivent pour vérifier notamment l’innocuité de certaines thérapeutiques sur l’humain. Le Dr Giacobini est optimiste et espère que dans les 5 à 10 années à venir, de nouveaux traitements voient le jour.
Elise Rouvrais, naturopathe et chargée de comité scientifique pour l’Association Esp’Opk
Créé en novembre 2018, l’Association Esp’Opk œuvre depuis trois ans pour une reconnaissance de la pathologie et de ses symptômes, en apportant un accompagnement aux personnes diagnostiquées, en effectuant la curation d’informations vérifiées, en informant et sensibilisant le grand public et les instances décisionnelles au syndrome des ovaires polykystiques, et en soutenant la recherche.
Nous remercions le Dr Paolo Giacobini, directeur de chercheur à l’Inserm de Lille et spécialisé en neuro-endocrinologie et Biologie de la reproduction, pour sa disponibilité et sa contribution.
Pour mieux vivre avec le SOPK, n’hésitez pas à prendre RDV en naturopathie, en complément d’un suivi médical conventionnel.
Sources et lectures :
Livres :
Le corps humain comment ça marche ? – Le courrier du livre
La symphonie du vivant – Joël De Rosnay- LLL
Site internet :
Inserm : Syndrome des ovaires polykystiques (SOPK)
Inserm : Epigénétique, un génome plein de possibilités !
Inserm : Transmission du SOPK de mère en fille : l’épigénétique en cause
Inserm : Infertilité : un mécanisme cérébral totalement inédit
CEA : Tout s’explique : qu’est-ce que l’épigénétique ?
Etudes :
(1) Mimouni NEH, Paiva I, Barbotin AL, Timzoura FE, Plassard D, Le Gras S, Ternier G, Pigny P, Catteau-Jonard S, Simon V, Prevot V, Boutillier AL, Giacobini P. Polycystic ovary syndrome is transmitted via a transgenerational epigenetic process. Cell Metab. 2021 Mar 2;33(3):513-530.e8. doi: 10.1016/j.cmet.2021.01.004. Epub 2021 Feb 3. PMID: 33539777; PMCID: PMC7928942.
(2) Cimino I, Casoni F, Liu X, Messina A, Parkash J, Jamin SP, Catteau-Jonard S, Collier F, Baroncini M, Dewailly D, Pigny P, Prescott M, Campbell R, Herbison AE, Prevot V, Giacobini P. Novel role for anti-Müllerian hormone in the regulation of GnRH neuron excitability and hormone secretion. Nat Commun. 2016 Jan 12;7:10055. doi: 10.1038/ncomms10055. PMID: 26753790; PMCID: PMC4729924.




2 Comments
Luna
25 mars 2022 at 0h27Merci pour votre site si bien informé.
Il y a 6 ans ont se sentait bien seule.
Cet article est particulièrement positif quant à un traitement adapté au SOPK, ça donne de l’espoir.
De mon côté avant : acné, pilosité, Testo et cortisol élevé, LSH/FH inversé (on m’a dit que j’allais me transformer en mec.. Ou mourrir d’un cancer.. À 24 ans j’etais seule face à tout ça et ça m’a bien choquée. J’étais tellement mal accompagnée, tout le monde me disait que c’etait dans ma tête, aucunes infos, sacré époque !).
Aujourd’hui je prends androcur en micro micro dose, sport, medit, et alimentation. Acné et pilosité stable, Testo qui a diminué et cortisol toujours limite. Donc plutôt super vivable par rapport à avant, même si j’aimerais me passer d’androcur. (Ai fait un IRM d’ailleurs, RAS.)
Mais quand y’en à plus y’en à encore 🤪, je viens d’avoir 30 ans et commence à avoir beaucoup de cellulite qui s’accumule partout (du à exces cortisol selon moi) alors que je suis plutôt grande mince, les ongles mou et cassants et surtout un fuckin Melasma (pourtant pas d’exces d’oestrogene) moi qui adore le soleil.. 😪.
Je pensais faire un tour du côté de l’insulino-résistance et éventuellement des carences. Qu’en pensez vous ? Avez vous d’autres pistes ? Surtout pour le Melasma.
Dois je me tourner vers un nutritionniste ou plutôt diabetologue ? (A savoir que Andocrino et Dermato j’ai donné, disent ne rien pouvoir faire, à part si tumeur ou laser peeling sur la peau 🤣).
La médecine parallèle comme le magnétisme m’a beaucoup aidé.
J’avoue également avoir repris un peu la viande rouge et le fromage alors que j’avais totalement arrêté. Je pense recontinuer en ce sens.
En tout cas, vivement dans 5/10 ans ou avant je l’espère !!! Amen 🙏
Elise Rouvrais
26 mars 2022 at 16h09Bonjour Luna,
Je vous remercie pour votre adorable message et pour votre partage d’expérience. Je suis sincèrement désolée d’apprendre que vous avez été mal accompagnée lors du diagnostic de votre SOPK et que vous ayez entendu de telles horreurs ! Une grande partie de mon travail consiste à tordre le coup des idées reçues sur les pathologies hormonales mais aussi de sensibiliser un maximum le grand public à ces troubles.
Effectivement, il existe différentes pistes pour les problèmes que vous avez évoqués. Malheureusement, je ne peux vous conseiller sans faire + ample connaissance avec vous. Je vous recommande de prendre une consultation à mon cabinet ou en visio si vous le souhaitez. J’accompagne de nombreuses femmes qui présentent un SOPK, j’en ai fait ma spécialité! La résistance à l’insuline et l’équilibre alimentaire sont des leviers très importants sur lesquels nous pourrons travailler.
Bien à vous.
Elise